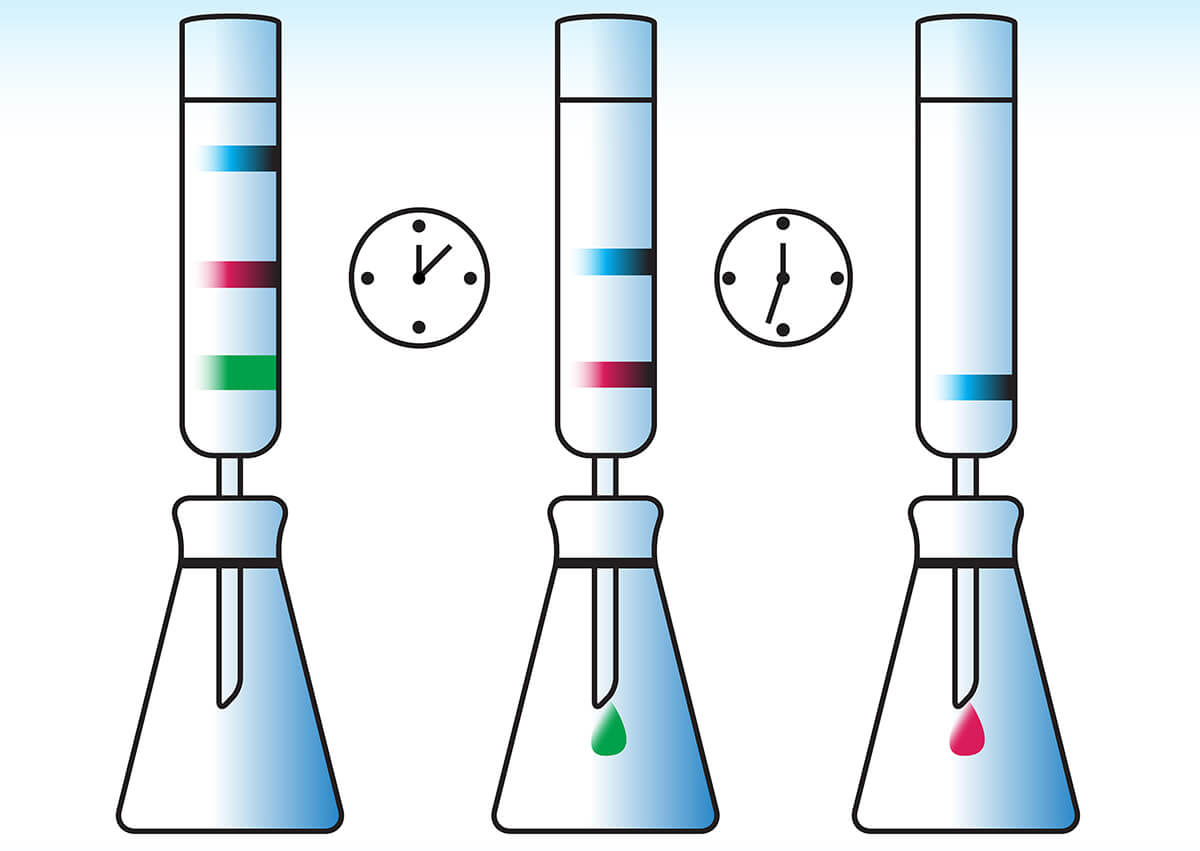
Wat is chromatografie?
Chromatografie is een bekende scheidingsmethode om mengsels te scheiden of om bepaalde stoffen in het mengsel aan te tonen. Er zijn verschillende vormen van chromatografie. Elke vorm is gebaseerd op het principe van een mobiele en een stationaire fase. In dit artikel lees je welke vormen van chromatografie er allemaal zijn en hoe deze precies werken.

Papierchromatografie

Een bekende vorm van chromatografie is papierchromatografie. Hiermee kun je bijvoorbeeld bepalen welke stoffen er in een mengsel zitten. Bij papierchromatografie wordt het papier met de onderkant in een loopvloeistof (water of methanol) gedoopt en na enige tijd trekt de loopvloeistof in het papier. De loopvloeistof gaat dan omhoog lopen. Deze loopvloeistof bevindt zich in de mobiele fase van het traject. De ene stof lost beter op in het oplosmiddel dan de andere stof. Papierchromatografie is onder andere gebaseerd op een verschil in oplosbaarheid. Hoe beter de stoffen in de loopvloeistof oplossen, hoe verder het wordt meegenomen. Deze stoffen zullen een grotere afstand leggen op het papier. Nu is er nog een fase aanwezig die de afgelegde afstand beïnvloedt, namelijk de stationaire fase. Bij papierchromatografie bevindt het papier zich in de stationaire fase. Hoe beter de stoffen aan het papier hechten (hogere affiniteit), hoe minder ver het uiteindelijk wordt meegenomen door de loopvloeistof. Deze aanhechting remt de stoffen dus als het ware af. Papierchromatografie scheidt dus stoffen op basis van twee stofeigenschappen: de oplosbaarheid in de loopvloeistof (mobiele fase) en het aanhechtingsvermogen aan het oppervlak (stationaire fase). Het uiteindelijke resultaat noemt men een chromatogram.
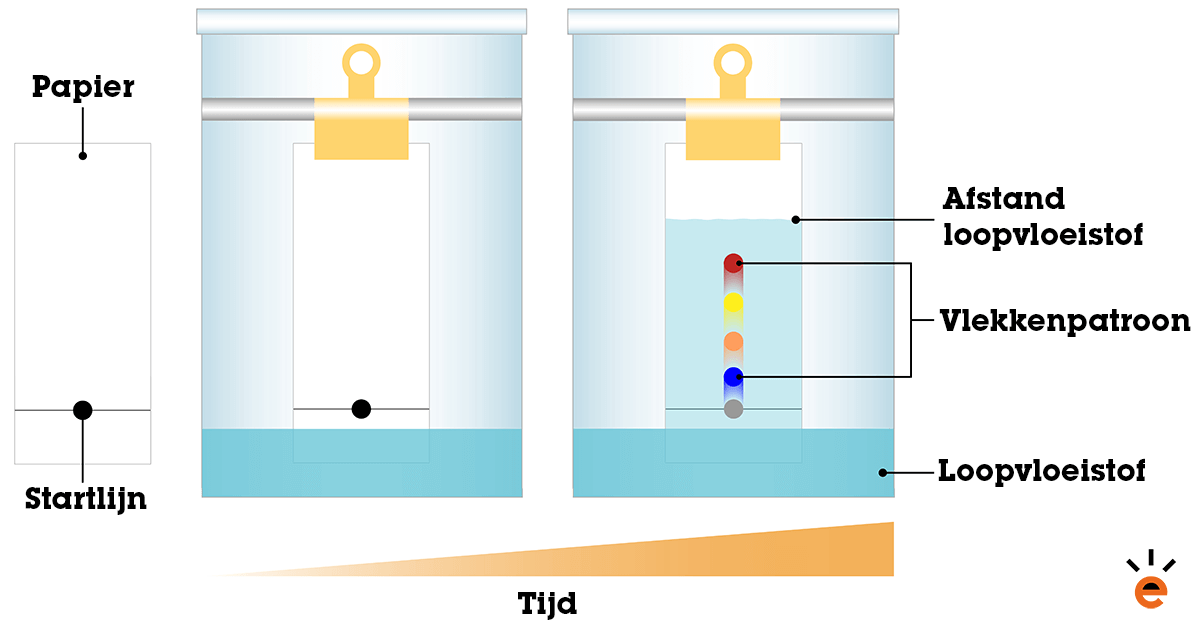
Op de afbeelding is te zien dat de stoffen verschillende afstanden afleggen ten opzichte van de startlijn. Deze afstand wordt gedeeld door de afstand die de loopvloeistof uiteindelijk aflegt en dit noemt men de loopafstand of Rf-waarde. Deze kun je berekenen met de volgende formule:
Rf = afgelegde weg van bepaalde stof / afgelegde weg van de loopvloeistof (het vloeistoffront)
Omdat de Rf-waarde per stof verschillend is, kun je de verschillende stoffen in het mengsel onderscheiden.
Over het algemeen is de regel: hoe beter een stof oplost in de loopvloeistof, hoe verder deze omhoog loopt met het vloeistoffront.
Dunnelaagchromatografie

Soms wordt er in plaats van papier gebruikgemaakt van een verharde ondergrond met een extra adsorberend laagje, dan heet het dunnelaagchromatografie. In het Engels wordt dit thin layer chromatography genoemd. De stationaire fase verschilt dus met die van papierchromatografie. Vaak wordt er glas, aluminium of kunststof als ondergrond gebuikt met als absorberend laagje een silicagel, aluminiumoxide of cellulose. Het principe is verder hetzelfde als bij papierchromatografie. De scheidingsmethode is nog steeds berust op het verschil in oplosbaarheid in de loopvloeistof en de affiniteit voor in dit geval de extra adsorberende laag.
In laboratoria wordt er gebruikgemaakt van dunnelaagchromatografie om kwalitatieve en kwantitatieve analyses uit te voeren. Kwalitatieve analyses worden gedaan als men erachter wilt komen welke verschillende stoffen er in een mengsel zitten. Hierbij wordt zowel bij papierchromatografie als bij dunnelaagchromatografie gebruikgemaakt van de stof specifieke Rf-waarde. Als deze waardes onderzocht zijn, kan men de verschillende stoffen in het mengsel identificeren. Ook kan men kwalitatieve analyses uitvoeren, dit betekent dat men de hoeveelheid van elke stof in een mengsel onderzoekt. Het is mogelijk om de hoeveelheid stof te bepalen aan de hand van de hoeveelheid (intensiteit) kleur van een specifieke stof. Hoe meer stof er aanwezig is, hoe intenser de kleur van die stof. Echter is dit moeilijk met het blote oog te zien. Daarom is het mogelijk om het papier of het plaatje te onderzoeken met een andere techniek, bijvoorbeeld met spectrofotometrie.

Gaschromatografie
Gaschromatografie is een vorm van chromatografie die werkt met een machine: de gaschromatograaf. Bij gaschromatografie worden stoffen gescheiden op basis van kookpunt. Ook gaschromatografie is gebaseerd op de oplosbaarheid in de mobiele fase en het aanhechtingsvermogen aan de stationaire fase.
Nu bevindt het mengsel (gas) zich in een draaggas. Dit is de mobiele fase van het traject. Het draaggas stroomt langs de meterslange gaschromatografische kolom waar het vervolgens aan vasthecht (stationaire fase). De ene gassoort hecht beter aan de stationaire fase dan de andere gassoort. Uiteindelijk komen alle deeltjes aan in de detector, echter met een bepaalde vertraging. De deeltjes die meer worden afgeremd, hebben een hogere vertraging en zullen dus later gedetecteerd worden. De tijd die nodig is voor een gas om aan te komen bij de detector noemt men de retentietijd. De retentietijd verschilt per stof en is ook afhankelijk van de omstandigheden. Bij het gebruiken van 2 verschillende machines kan de retentietijd dus verschillen. In het algemeen verdampen moleculen met een lager kookpunt sneller, en komen dus eerder aan bij de detector (en hebben daarmee een kortere retentietijd. Als een stof de detector passeert dan krijg je een piek in je gaschromatogram. De oppervlakte onder de piek (de piekoppervlakte) geeft hierbij ook de hoeveelheid stof aan. Gaschromatografie kan op verschillende worden toegepast. Bijvoorbeeld bij onderzoek naar doping onder sporters, kan de urine van een sporter op basis van gaschromatografie onderzocht worden.
Kolomchromatografie
Stel je voor: je wilt twee stoffen in een oplossing van elkaar scheiden. Dan kun je dat ook doen met kolomchromatografie. Hierbij wordt er, zoals de naam al zegt, gebruikgemaakt van een lange kolom.
Het mengsel van de twee verschillende stoffen wordt bovenin geplaatst. Hier wordt een oplosmiddel langs gegoten waardoor het mengsel door de kolom gaat stromen (mobiele fase). Zodra het mengsel gaat stromen gaat het langs een vast dragermateriaal waar het mengsel aan vasthecht (stationaire fase). Een van de stoffen heeft een grotere affiniteit voor het vaste dragermateriaal, waardoor deze in de kolom blijft hangen. De andere stof zal doorstromen en uiteindelijk in de beker terechtkomen. Voordat het de beker bereikt gaat het door een poreus glazen schijfje die ervoor dient om te voorkomen dat het dragermateriaal naar beneden zal stromen. Het kan dus wel de stof uit het mengsel doorlaten.
Video
Wil je meer weten over chromatografie? Kijk dan onderstaande video van scheikundeleraar Sieger Kooij, die het onderwerp nog een keer duidelijk uitlegt.