Molecuulformules en structuurformules
Er bestaan verschillende manieren om een stof te benoemen. Elke stof heeft een naam, een molecuulformule en een structuurformule. In dit artikel worden de molecuulformule en de structuurformule uitgelegd en wordt er benoemd wanneer je een structuurformule het best kan gebruiken.
Molecuulformule

Een molecuulformule is een opsomming van de atomen in een molecuul. Een molecuulformule van een stof wordt gemaakt door het soort atoom te benoemen en daarna in subscript te vermelden hoeveel van dit soort atomen het molecuul bevat. Een makkelijk voorbeeld is waterstof, H2. Dit molecuul bestaan uit alleen H-atomen, aangezien deze als enige vermeld zijn in de molecuulformule. Uit het subscript 2 is op te maken dat dit molecuul bestaat uit 2 H-atomen.
Voor het opstellen van molecuulformules van koolwaterstoffen, is de conventie dat eerst de C-atomen benoemd worden, daarna de H-atomen, de O-atomen en daarna de rest van de soorten atomen in het molecuul, zoals bijvoorbeeld de halogenen. Bijvoorbeeld voor glucose C6H12O6.
Een ander voorbeeld is methanol. Methanol bestaat uit 1 C-atoom, 4 H-atomen en 1 O-atoom. Een voor de hand liggende molecuulformule is dus CH4O. Met een molecuulformule kan ook iets gezegd worden over de structuur van een molecuul. Methanol is een koolstofatoom met een gebonden -OH groep. Het aangeven daarvan in de molecuulformule gaat als volgt: CH3OH. Hiermee wijkt deze molecuulformule af van de conventie, maar voor een goede reden, namelijk het tonen van de structuur van het molecuul.
Een makkelijke regel voor het opstellen van een molecuulformule voor verzadigde koolstofketens, zoals pentaan en octaan, is CnH2n+2, waarbij n het aantal koolstofatomen in de keten is. Voor een koolstofketen met 1 dubbele binding, zoals propeen en hexeen, is de molecuulformule CnH2n.
Hieronder staan een paar voorbeelden van veelvoorkomende molecuulformules:
- Ammoniak: NH3
- Azijnzuur: CH3COOH
- Butaan: C4H10
- Ethaan: C2H6
- Fosforzuur: H3PO4
- Glucose: C6H12O6
- Koolstofdioxide: CO2
- Methaan: CH4
- Propaan: C3H8
- Salpeterzuur: HNO3
- Stikstofdioxide: NO2
- Water: H2O
- Waterstofchloride: HCl
- Waterstofperoxide: H2O2
- Zwavelzuur: H2SO4
Structuurformule

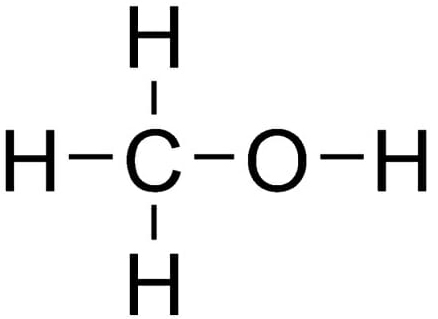
Een makkelijkere manier om de structuur van een molecuul aan te geven is met een structuurformule. Hierin worden niet alleen de soorten atomen en hun hoeveelheden aangegeven, maar ook hun positie in het molecuul en de bindingen tussen de atomen. Voor het voorbeeld methanol is de structuurformule:
Figuur 1: de structuurformule van methanol
In structuurformules wordt de soort binding tussen atomen ook aangegeven. Er bestaan enkele bindingen, dubbele bindingen en zelfs drievoudige bindingen tussen atomen. Een voorbeeld van een stof met een dubbele binding is etheen.
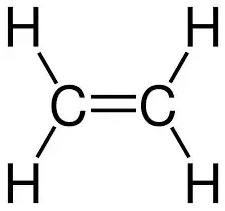
Figuur 2: de structuurformule van etheen
Hier wordt de dubbele binding aangegeven met dubbele strepen. Hiervan is de molecuulformule C2H4.
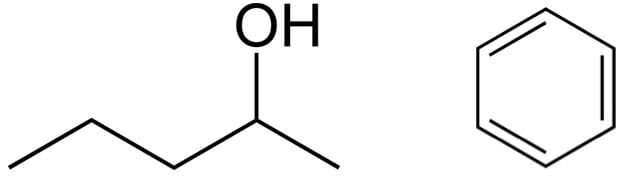
In een structuurformule mogen de H-atomen gebonden aan een C-atoom vaak weggelaten worden, maar de H-atomen aan andere soorten atomen, zoals bijvoorbeeld O-atomen of N-atomen, moeten altijd benoemd worden. Ook mag de letter C weggelaten worden voor het aangeven van koolstofatomen. Wanneer dit het geval is, spreekt men van een skeletstructuur. Voor de moleculen 2-pentanol (C5H9OH) en benzeen (C6H6) zien de skeletstructuren er als volgt uit:
Figuur 3: de skeletstructuur van 2-pentanol (links) en benzeen (rechts)
In een skeletstructuur worden de koolstofatomen niet aangegeven met de letter C, maar zitten er op de hoeken tussen de bindingen koolstofatomen. De binding tussen het zuurstof- en het waterstof atoom mag weggelaten worden. Ook de H-atomen aan de koolstofatomen worden meestal weggelaten. Dit is handig voor het simpel en overzichtelijk weergeven van moleculen, vooral als de moleculen groter en gecompliceerder worden.
Wanneer gebruik je de structuurformule?
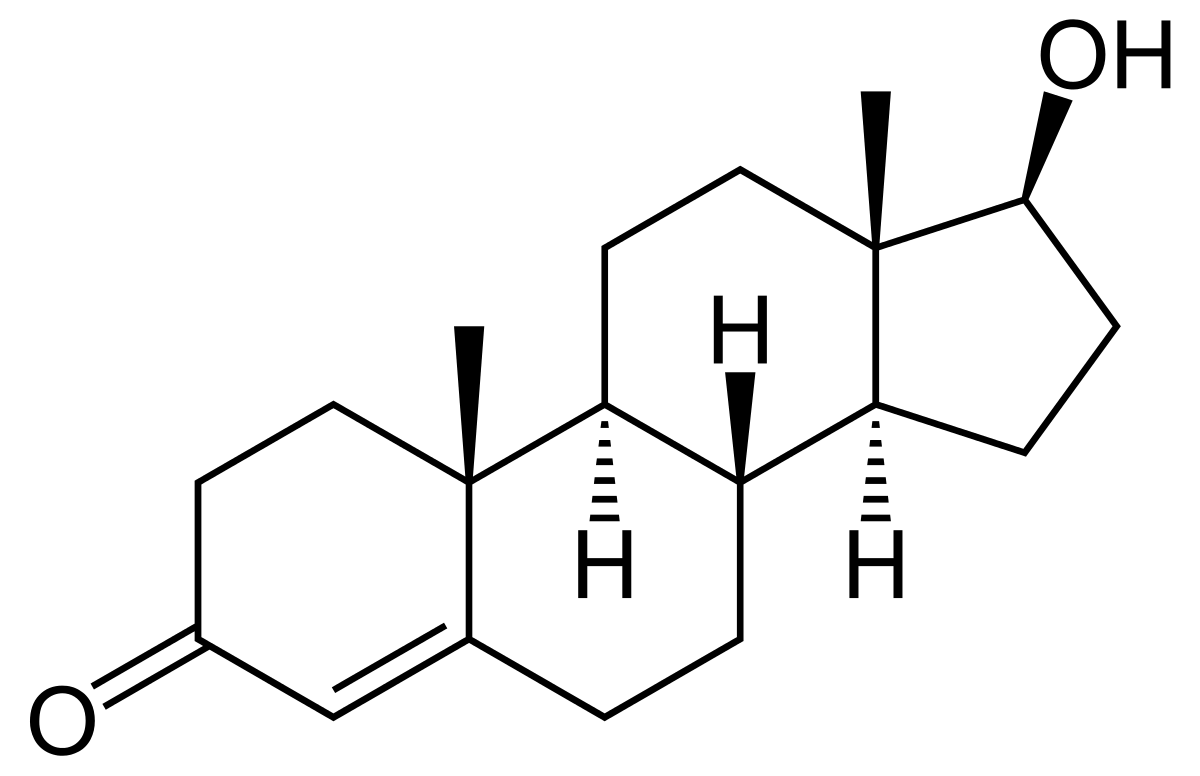
Uit de molecuulformule van etheen zou nog op te maken zijn dat er een dubbele binding aanwezig moet zijn tussen de koolstofatomen. Wanneer de stof veel complexer is, zoals hormonen of vetten, is dit niet meer het geval en zijn er structuurformules nodig om te achterhalen hoe een molecuul eruitziet. Neem bijvoorbeeld testosteron. De molecuulformule van dit hormoon is C19H28O2. Met deze hoeveelheid atomen zijn er heel veel mogelijke soorten structuurformules, oftewel isomeren. Isomeren, stoffen met hetzelfde aantal en soort atomen maar met een andere structuur, hebben dezelfde molecuulformule maar een andere structuurformule. De juiste structuur van de stof is dan niet op te maken uit alleen de molecuulformule. De structuurformule van testosteron, getekend op de manier van de skeletstructuur, is:
Figuur 4: de structuurformule van testosteron
Iets nieuws in deze structuurformule wat nog niet eerder getoond is, zijn de bindingen die van smal naar breed lopen, volledig zwart of gestreept. Deze aanduidingen betekenen dat de binding naar voren (volledig zwart) of naar achteren (gestreept) staat ten opzichte van het molecuul. De H-atomen aan deze bindingen worden wel genoemd, aangezien deze belangrijke informatie tonen over de structuur van het molecuul. Hierdoor wordt er meer duidelijk over de ruimtelijke 3D structuur van het molecuul.
Oftewel: in een molecuulformule worden alleen de atomen en hun hoeveelheid in het molecuul genoemd, en een structuurformule geeft ook opheldering over de positie van de atomen en de bindingen tussen atomen. In een molecuulformule kan aan de hand van de volgorde van de atomen in de formule soms iets worden opgemaakt over de structuur. In een structuurformule kunnen alle atomen en bindingen benoemd worden, of kan een versimpelde structuur worden getekend om complexe moleculen makkelijker te maken. Dit heet een skeletstructuur. Één molecuulformule kan meerdere mogelijke structuurformules hebben, dit heten isomeren. Als er meer bekend gemaakt wil worden over de precieze ruimtelijke structuur van een molecuul, moet een structuurformule gebruikt worden.
Structuurformules tekenen (video)
Wil je weten hoe je structuurformules moet tekenen? Kijk dan onderstaande video van Scheikundelessen.