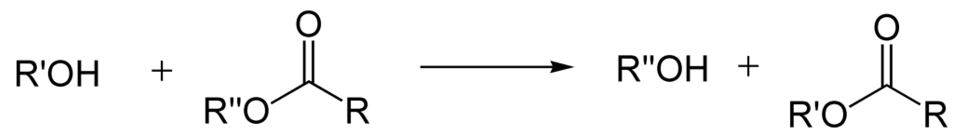Esters
Wanneer een alcohol en een carbonzuur met elkaar reageren, ontstaat een ester. Maar wat is een ester nu precies? En hoe werkt het met de naamgeving van esters? Je leest het in dit artikel.

Wat is een ester?

Een ester is een chemische koolstofverbinding met een bepaalde karakteristieke groep. Esters worden meestal gevormd door de reactie tussen een carbonzuur en een alcohol, maar kunnen ook door andere reacties gemaakt worden, zoals bijvoorbeeld met een zuurchloride in plaats van een carbonzuur. Esters zijn vooral geur- en smaakstoffen en bevinden zich onder andere veel in fruit, zoals in ananas, appels, peren en aardbeien. Daarnaast worden esters ook gebruikt bij het maken van bijvoorbeeld verf, lijm, inkt en parfums.
De functionele groep die zich in esters bevindt is deze:
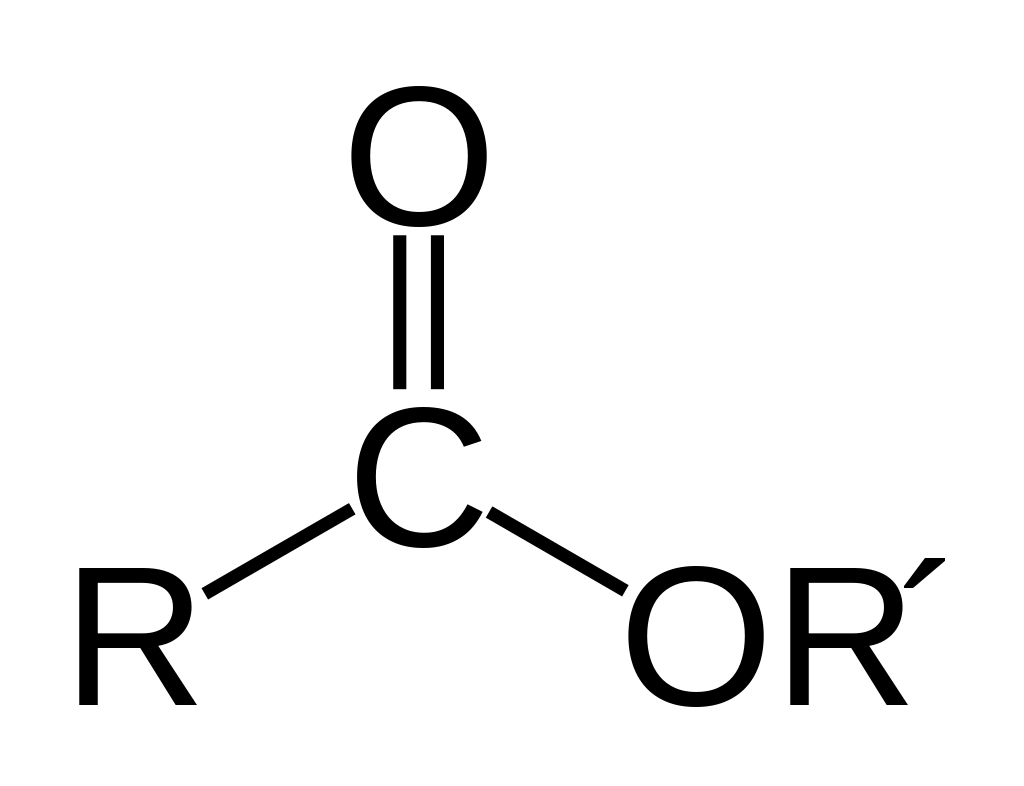
Deze functionele groep heet de estergroep. De R substituent kan hier zowel een koolstofatoom of koolstofketen zijn, als een waterstofatoom. De R’ substituent moet een koolstofatoom of koolstofketen zijn, anders is deze verbinding geen esterverbinding. Als R’ namelijk een H-atoom was geweest, was dit de functionele groep van een carbonzuur.
Wil je meer weten over wat een ester precies is? Kijk dan onderstaande video van scheikundeleraar Sieger Kooij.
Eigenschappen van een ester

Esters bevatten geen waterstofburgvormende groepen, zoals -OH of -NH groepen. De ester bevat wel een H-brugontvangende groep, namelijk het dubbelgebonden zuurstofatoom. Daarnaast is een ester redelijk apolair, in vergelijking met bijvoorbeeld carbonzuren of alcoholen. Hierdoor is een ester niet erg hydrofiel, en lossen esters slecht op in water.
Omdat een ester geen waterstofbrugvormende groepen bevat, kan het met zichzelf geen bruggen maken. Dit betekent dat de Vanderwaalsinteracties de grootste bijdrage hebben aan de intermoleculaire interacties tussen esters. Hierdoor zijn de kookpunten van esters vrij laag, ongeveer even hoog als de kookpunten van alkanen met hetzelfde moleculaire gewicht.
Het ontstaan van esters

Een ester ontstaat meestal door de reactie tussen een alcohol en een carbonzuur. Deze reactie heet een Fischer-verestering of Fischer-esterificatie. Deze reactie is ook een condensatiereactie, omdat er water vrijkomt tijdens de reactie.
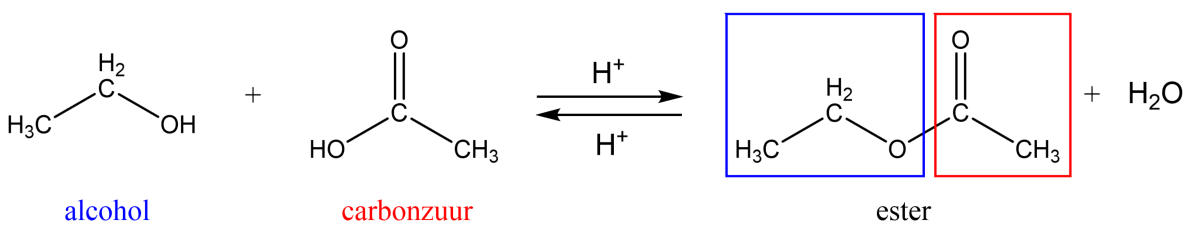
De reactie tussen een specifiek alcohol en carbonzuur verloopt alleen onder de juiste omstandigheden, bijvoorbeeld bij de juiste temperatuur en druk. Daarnaast is er meestal een katalysator nodig om de reactie op gang te brengen of te versnellen. Dit is meestal een zuur, zoals zwavelzuur. Hieronder is een voorbeeld esterificatie reactie te zien tussen een alcohol en een zuur:
Het blauwe deel van de ester is afkomstig van het alcohol, terwijl het rode deel van de ester afkomstig is van het carbonzuur. Deze reactie tussen een alcohol en een carbonzuur is een evenwichtsreactie en kan dus ook de andere kant op reageren. Dit gebeurt ook met een zuur als katalysator, zoals zwavelzuur. Deze omgekeerde reactie heet een hydrolysereactie.
Een esterficatie reactie kan ook gebeuren tussen een zuurchloride en een alcohol. Een zuurchloride heeft in plaats van een -OH groep in het carbonzuur, een -Cl groep:
Een zuurchloride reageert meestal sneller dan een carbonzuur en deze reactie is niet in evenwicht, maar onomkeerbaar. Dit maakt het scheiden van het eindproduct makkelijker.
Een ester kan ook gemaakt worden door een omesteringsreactie, ook wel transesterificatie genoemd. Hierbij wordt de alkylgroep, die afkomstig is van de alcohol van een al bestaande ester, omgewisseld met een ander alcohol, zoals in de reactie hieronder.
Naamgeving
De naamgeving van esters is mogelijk op meerdere manieren. De makkelijkste manier is het benoemen van de twee componenten van de ester. Bijvoorbeeld, voor bovenstaande reactie tussen ethanol en ethaanzuur, is de naam van de gevormde ester ‘de ester van ethanol en ethaanzuur’. Deze naamgeving wordt vaker gebruikt voor ingewikkelde esters met vertakkingen of ingewikkelde functionele groepen, omdat de systematische naam dan te gecompliceerd wordt.
Daarnaast is er ook de systematische IUPAC-naamgeving voor het naamgeven van esters. Deze bestaat uit eerst de naam van de alcohol, met daarachter de naam van het zuur, beide met andere uitgangen. De -anol uitgang van de alcohol wordt vervangen door -yl en de -zuur uitgang van het zuur wordt vervangen met -oaat. In het algemeen is de naamgeving van een ester dus alkyl alkanoaat. De ester van methanol en ethaanzuur wordt dus: methyl ethanoaat.
Voorbeelden naamgeving
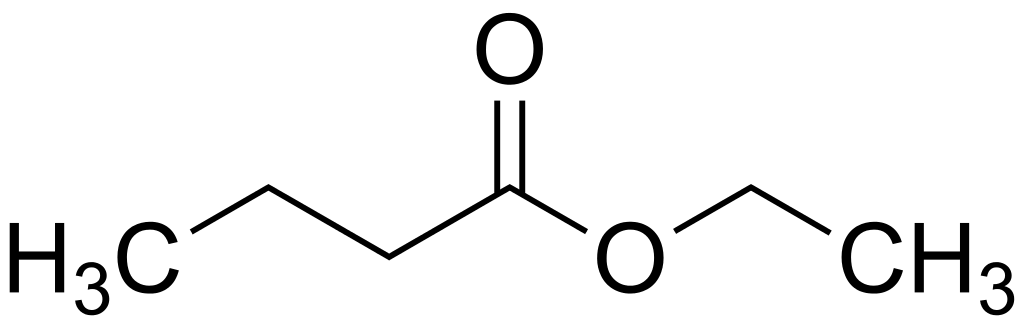
Onderstaande ester bestaat uit het zuur butaanzuur en de alcohol ethanol. Hierdoor is de systematische naam van deze ester ethyl butanoaat. Deze ester komt voor in banaan, ananas en peer. Hij heeft een op een ananas lijkende geur.
Onderstaande ester bestaat uit het zuur ethaanzuur en een vertakt alcohol, 2-methylpropanol. De systematische naam van deze ester is dus 2-methylpropyl ethanoaat. Een veel gebruikte triviale naamgeving voor ethanoaat is acetaat, en voor 2-methylpropyl wordt vaak isobutyl gebruikt. Deze ester kan dus ook isobutyl acetaat genoemd worden. Deze ester komt onder andere voor in kersen, aardbeien, peren en frambozen. Hij heeft een sterk fruitige geur.
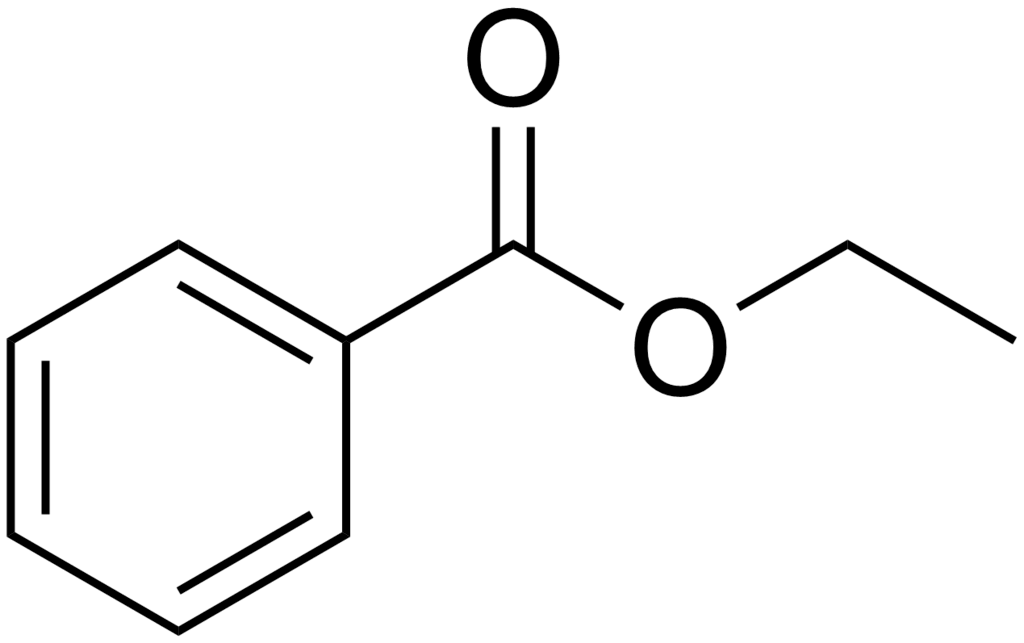
Onderstaande ester bevat een zuur met een functionele groep, namelijk een benzeen ring. Dit zuur heet benzoëzuur en in de systematische naamgeving van een ester wordt dit dan benzoaat. Het alcohol is ethanol, dus de systematische naamgeving van deze ester is ethyl benzoaat. Deze ester komt onder andere voor in papaya en perzik. Hij heeft een zoete fruitige geur.