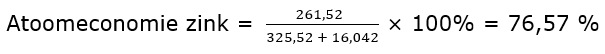Groene chemie

Wat is groene chemie?

Groene chemie is de tak binnen de chemie waarbij men als eerste kijkt naar duurzaamheid.
Misschien heb je er ooit wel iets over gelezen, maar het wordt steeds duidelijker dat grondstoffen die op de aarde beschikbaar zijn, op kunnen raken. Daarom wordt het steeds belangrijker om de aarde te beschermen door rekening te houden met het milieu. Bedrijven en fabrieken gaan steeds beter letten op de duurzaamheid van de processen en de technologie die ze gebruiken. Dit doen ze in principe door zo weinig mogelijk energie te verbruiken, hernieuwbare grondstoffen te gebruiken en het mogelijk maken om een eindproduct te kunnen recyclen. Bij een recyclebaar product kun je denken aan bijvoorbeeld krantenpapier.
Als een product recyclebaar is, gaan de grondstoffen uiteindelijk vaker en langer mee. Er zijn echter nog veel producten die meteen worden weggegooid. Bij groene chemie wordt er bedoeld dat we voor de toekomstige generaties moeten zorgen en daarom wordt onder andere recyclen steeds belangrijker. Het beste zou natuurlijk zijn als alle grondstoffen die je gebruikt om een product te maken weer opnieuw gebruikt kunnen worden. Het streven naar het maken van 100% recyclebare producten noemt men het cradle-to-cradle (C2C) principe.
Wat zijn de 12 principes van groene chemie?

Er zijn 12 principes van groene chemie:
1. Preventie
Vorming van afval moet zoveel mogelijk worden voorkomen.
2. Atoomeconomie
Het eindproduct bevat zoveel mogelijk atomen van de in het proces gebruikte stoffen. Oftewel, de grondstoffen moeten dus zo efficiënt mogelijk worden gebruikt.
3. Minder schadelijke chemische productiemethoden
Productieprocessen moeten zodanig worden ontworpen dat het mens en milieu zo weinig mogelijk schaadt.
4. Ontwikkelen van minder schadelijke chemische stoffen
Let er bij de ontwikkeling van producten op dat ze doen wat ze moeten doen, met zo weinig mogelijk schade aan mens en milieu.
5. Veiliger oplosmiddelen
Vermijd tijdens de productie zoveel mogelijk het gebruik van oplosmiddelen.
6. Energie-efficiënt ontwerpen
De energie die nodig is om een reactie uit te voeren moet met het oog op vermindering van kosten en milieuschade worden verlaagd. Probeer daarom indien mogelijk processen uit te voeren bij relatief lage temperaturen en lage drukken. Daarnaast moet de energie die gebruikt wordt bij een productieproces zoveel mogelijk worden hergebruikt.
7. Gebruik van hernieuwbare grondstoffen
Grondstoffen moeten zoveel mogelijk hernieuwbaar zijn (bijvoorbeeld planten).
8. Reacties in weinig stappen
Reacties waar veel stappen voor nodig zijn, moeten worden vermeden. Als er namelijk veel stappen in een proces plaatsvinden, betekent dat dat er meer uitgangsstoffen nodig zijn en daarmee ontstaat er meer vervuiling.
9. Katalysator
Reacties die gebruikmaken van een katalysator zijn efficiënter dan niet-gekatalyseerde reacties.
10. Ontwerpen met het oog op afbraak
Ontwerp chemische producten waaruit bij afbraak stoffen ontstaan die niet giftig zijn en niet ophopen in het milieu.
11. Tussentijdse analyse met het oog op preventie van milieuverontreiniging
Door analysemethoden te gebruiken moet er gezorgd worden dat milieuverontreinigende (bij)producten worden ontdekt zodra ze vrijkomen.
12. Minder risicovolle chemie
Stoffen in een chemisch proces moeten dusdanig worden gekozen dat het risico op chemische ongelukken zo klein mogelijk is. Werk ook aan preventie op het gebied van brand en explosie.
Daarnaast zijn er nog andere belangrijke begrippen die aangeven hoe groen een productieproces precies is. Hier komt wat meer rekenwerk bij kijken, maar het zijn effectieve maatstaven voor de ‘groenheid’ van een productieproces. Om te kunnen rekenen met de volgende vergelijkingen, is het belangrijk dat je de reactievergelijking en de atoommassa’s van de aanwezige stoffen weet.
Video
Wil je nog deze stof nog eens uitgelegd hebben door Sieger kooij van Scheikundelessen? Bekijk dan onderstaande video!
Hoe reken je met de atoomeconomie?

Met de atoomeconomie berekenen we hoeveel van alle beginstoffen wordt omgezet in het gewilde product. Je krijgt uiteindelijk een percentage van je gewilde product ten opzichte van alle gebruikte beginstoffen. De formule is als volgt:
Hieronder staat de reactievergelijking voor de productie van zink. Je wil dus uiteindelijk zink overhouden.
4 ZnO + CH4 --> 4 Zn + CO2 + 2H2O
4 ZnO = 325,52 u
CH4 = 16,042 u
4 Zn = 261,52 u
CO2 = 44,01 u
2 H2O = 36,032 u
Om de atoomeconomie van zink te berekenen gaan we bovenstaande formule gebruiken. We willen alleen zink overhouden, dus deze vullen we bovenaan in de formule in. Alle beginstoffen zijn zinkoxide en methaan bij elkaar opgeteld.
Uiteindelijk is de atoomeconomie van zink dus 76,57%. Dat betekent dat 76,57% van al je beginstoffen wordt omgezet in je gewenste product en dat de rest, 23,43%, eigenlijk afval is.
Wat is het rendement?
Het rendement geeft aan welk deel van de beginstoffen wordt omgezet tot het gewilde product.
De atoomeconomie gaat ervan uit dat 100% van je beginstoffen wordt omgezet in de eindproducten. Echter gaat er nog wel eens wat verloren, bijvoorbeeld in de vorm van warmte. Sommige processen hebben een slecht rendement, wat inhoudt dat er een groot deel van de beginstoffen verloren gaat. Hierdoor ontstaat er meer afval, wat uiteindelijk slechter zal zijn voor het milieu. Hieronder vind je de berekening voor als het rendement van het productieproces van zink 75% zou zijn.
Dat betekent dat 57,42% van al je beginstoffen wordt omgezet in het gewenste product en dat de rest, 42,58%, afval is. Dit is bijna twee keer zoveel afval in vergelijking met de atoomeconomie.
Wat is de e-factor?
De e-factor (environmental factor) is een maatstaf voor de hoeveelheid afval per kilo product. Zo kun je bepalen hoe groen een productieproces echt is.
Een productieproces waarbij alleen water als afvalproduct eindigt, zal een veel lagere e-factor hebben dan een productieproces waarbij er heel veel koolstofdioxide in de lucht terecht komt. De e-factor bereken je als volgt:
De e-factor houdt dus automatisch rekening met het rendement van de reactie. Bij een kleine waarde zullen er weinig ongewenste stoffen aanwezig zijn in de eindproducten, wat daarom gewenst is. Bij een hoge waarde zullen er veel ongewenste stoffen aanwezig zijn in de eindproducten en dit is daarom ongewenst in de groene chemie.
Video
Wil je meer weten over het rekenen met de atoomeconomie en de groene chemie? Check dan onderstaande uitlegvideo: